Техника - молодёжи 1985-07, страница 39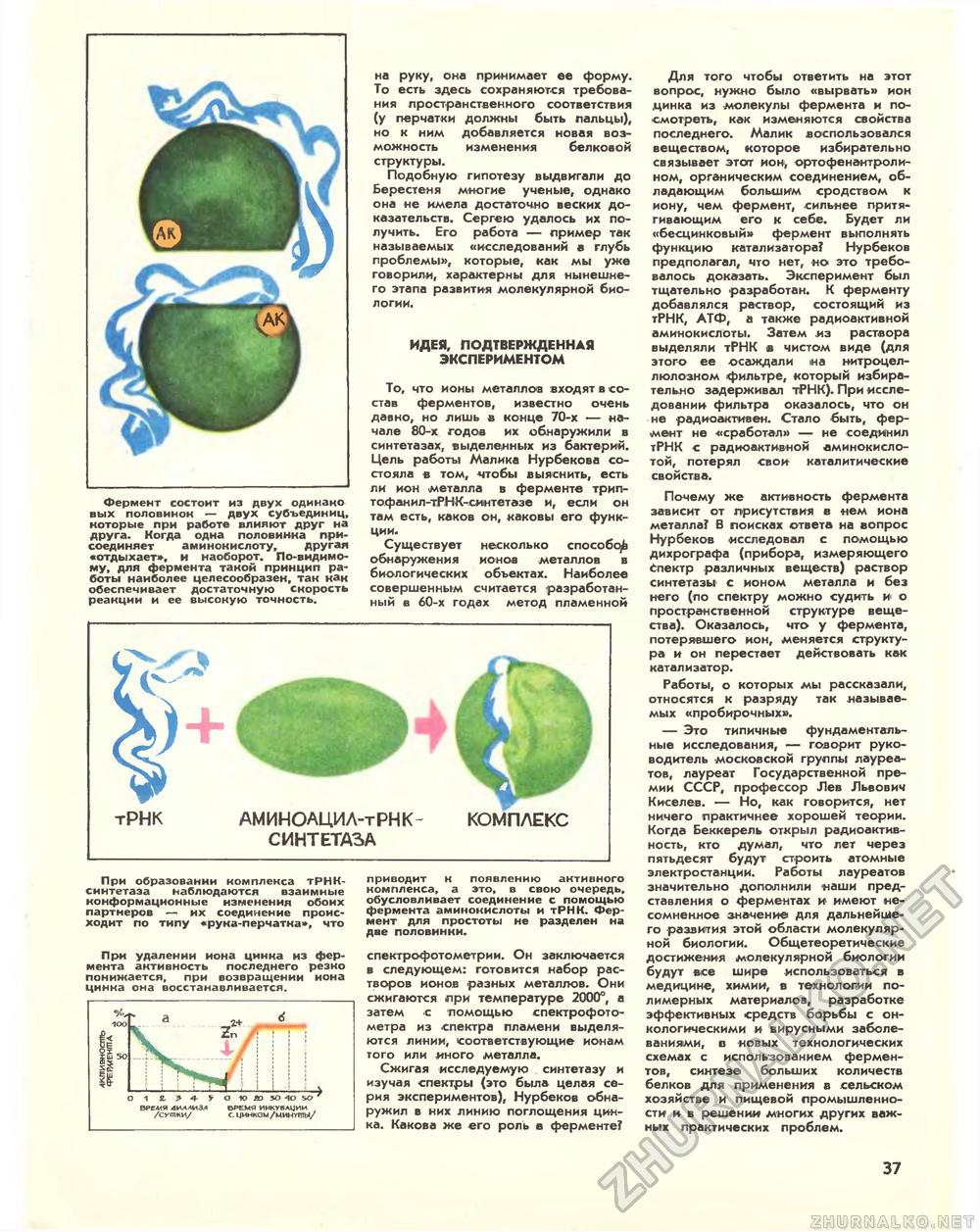
А to Фермент состоит из двух одинако вых половинок — двух субъединиц, которые при работе влияют друг на друга. Когда одна половинка присоединяет аминокислоту, другая «отдыхает», и наоборот. По-видимому, для фермента такой принцип работы наиболее целесообразен, так как обеспечивает достаточную скорость реакции и ее высокую точность. на руку, она принимает ее форму. То есть здесь сохраняются требования пространственного соответствия (у перчатки должны быть пальцы), но к ним добавляется новая возможность изменения белковой структуры. Подобную гипотезу выдвигали до Берестеня многие ученые, однако она не имела достаточно веских доказательств. Сергею удалось их получить. Его работа — пример так называемых «исследований а глубь проблемы», которые, как мы уже говорили, характерны для нынешнего этапа развития молекулярной биологии. ИДЕЯ, ПОДТВЕРЖДЕННАЯ ЭКСПЕРИМЕНТОМ То, что ионы металлов входят в состав ферментов, известно очень давно, но лишь в конце 70-х — начале 80-х годов их обнаружили в синтетазах, выделенных из бактерий. Цель работы Малика Нурбекова состояла в том, чтобы выяснить, есть ли ион металла в ферменте трип-тофанил-тРНК-синтетазе и, если он там есть, каков он, каковы его функции. Существует несколько способу обнаружения ионов металлов в биологических объектах. Наиболее совершенным считается разработанный в 60-х годах метод пламенной тРНК АМИНОАЦИА-тРНК-СИНТЕТАЗА КОМПЛЕКС При образовании комплекса тРНК-синтетаза наблюдаются взаимные конформационные изменения обоих партнеров — их соединение происходит по типу «рука-перчатка», что При удалении иона цинка из фермента активность последнего резко понижается, при возвращении иона цинка она восстанавливается. приводит к появлению активного комплекса, а это, в свою очередь, обусловливает соединение с помощью фермента аминокислоты и тРНК. Фермент для простоты не разделен на две половинки. спектрофотометрии. Он заключается в следующем: готовится набор растворов ионов разных металлов. Они сжигаются при температуре 2000°, а затем с помощью спектрофотометра из спектра пламени выделяются линии, соответствующие ионам того или иного металла. Сжигая исследуемую синтетазу и изучая спектры (это была целая серия экспериментов), Нурбеков обнаружил в них линию поглощения цинка. Какова же его роль в ферменте? Для того чтобы ответить на этот вопрос, нужно было «вырвать» ион .цинка из молекулы фермента и посмотреть, как изменяются свойства последнего. Малик воспользовался веществом, которое избирательно связывает этот ион, ортофенантроли-ном, органическим соединением, обладающим большим сродством к иону, чем фермент, сильнее притягивающим его к себе. Будет ли «бесцинковый» фермент выполнять функцию катализатора? Нурбеков предполагал, что нет, но это требовалось доказать. Эксперимент был тщательно разработан. К ферменту добавлялся раствор, состоящий из тРНК, АТФ, а также радиоактивной аминокислоты. Затем из раствора выделяли тРНК в чистом виде (для этого ее осаждали на нитроцел-люлозном фильтре, который избирательно задерживал тРНК). При исследовании' фильтра оказалось, что он не радиоактивен. Стало быть, фермент не «сработал» — не соединил тРНК с радиоактивной аминокислотой, потерял свои каталитические свойства. Почему же активность фермента зависит от присутствия в нем иона металла? В поисках ответа на вопрос Нурбеков исследовал с помощью дихрографа (прибора, измеряющего Спектр различных веществ) раствор синтетазы с ионом металла и без него (по спектру можно судить к о пространственной структуре вещества). Оказалось, что у фермента, потерявшего ион, меняется структура и он перестает действовать как катализатор. Работы, о которых мы рассказали, относятся к разряду так называемых «пробирочных». — Это типичные фундаментальные исследования, — говорит руководитель московской группы лауреатов, лауреат Государственной премии СССР, профессор Лев Львович Киселев. — Но, как говорится, нет ничего практичнее хорошей теории. Когда Беккерель открыл радиоактивность, кто думал, что лет через пятьдесят будут строить атомные электростанции. Работы лауреатов значительно дополнили наши представления о ферментах и имеют несомненное значение для дальнейшего развития этой области молекулярной биологии. Общетеоретические достижения молекулярной биологии будут все шире использоваться в медицине, химии, в технологии полимерных материалов, разработке эффективных средств борьбы с онкологическими и вирусными заболеваниями, в новых технологических схемах с использованием ферментов, синтезе больших количеств белков для применения в сельском хозяйстве и пищевой промышленности и в решении многих других важных практических проблем. 37 |








