Техника - молодёжи 1964-10, страница 10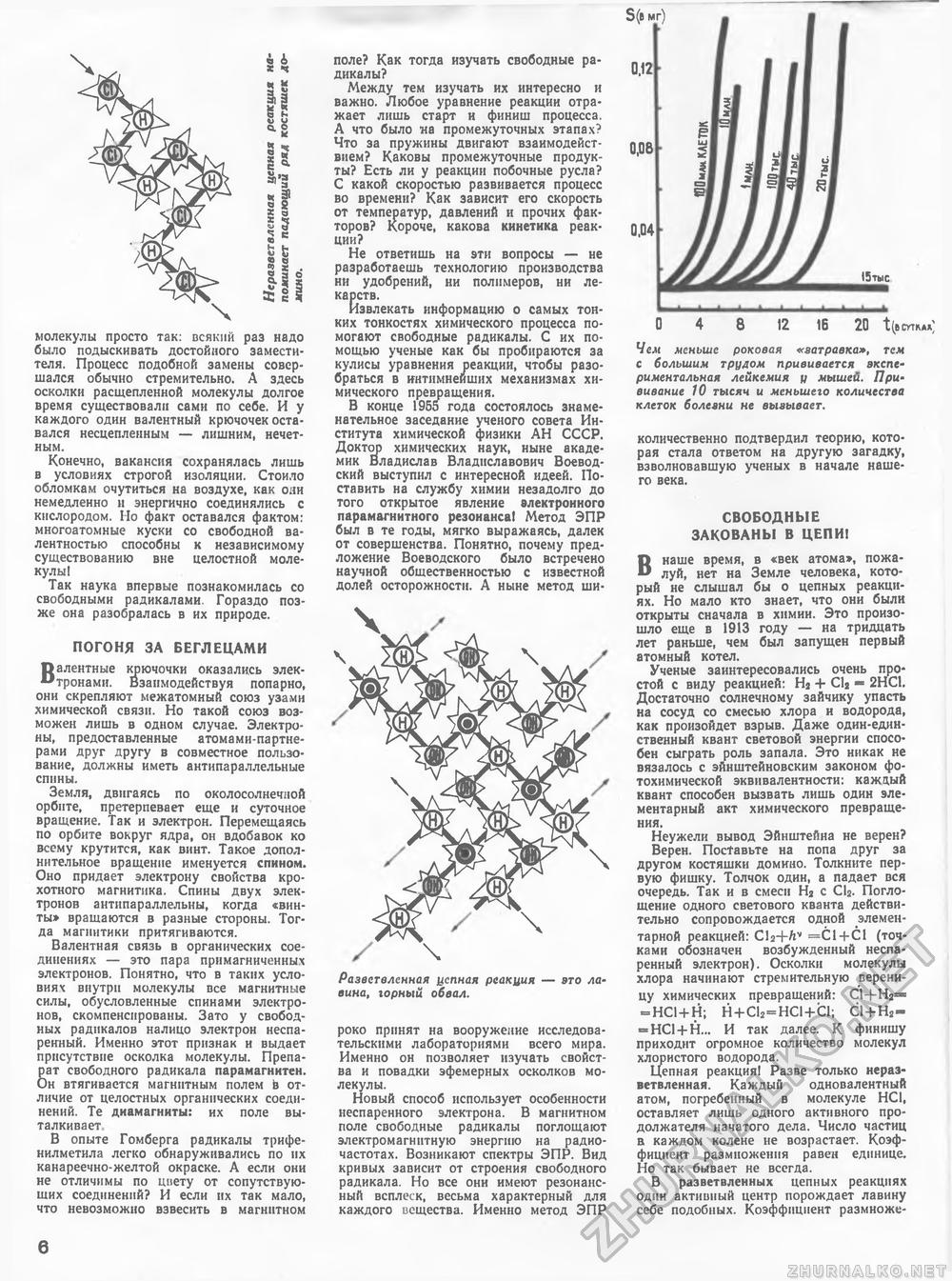
* * i! I * If II 5 * 11 |i! 33 с I молекулы просто так: всякий раз надо было подыскивать достойного заместителя. Процесс подобной замены совершался обычно стремительно. А здесь осколки расщепленной молекулы долгое время существовали сами по себе. И у каждого один валентный крючочек оставался несцеплеиным —- лишним, нечетным. Конечно, вакансия сохранялась лишь в условиях строгой изоляции. Стоило обломкам очутиться на воздухе, как они немедленно и энергично соединялись с кислородом. Но факт оставался фактом: многоатомные куски со свободной валентностью способны к независимому существованию вне целостной молекулы! Так наука впервые познакомилась со свободными радикалами. Гораздо позже она разобралась в их природе. ПОГОНЯ ЗА БЕГЛЕЦАМИ Палентные крючочки оказались элек-** тронами. Взаимодействуя попарно, они скрепляют межатомный союз узами химической связи. Но такой союз возможен лишь в одном случае. Электроны, предоставленные атомами-партнерами друг другу в совместное пользование, должны иметь антипараллельные спины. Земля, двигаясь по околосолнечной орбите, претерпевает еще и суточное вращение. Так и электрон. Перемещаясь по орбите вокруг ядра, он вдобавок ко всему крутится, как винт. Такое дополнительное вращение именуется спином. Оно придает электрону свойства крохотного магнитика. Спины двух электронов антипараллельны, когда «винты» вращаются в разные стороны. Тогда магнитики притягиваются. Валентная связь в органических соединениях — это пара примагниченных электронов. Понятно, что в таких условиях внутри молекулы все магнитные силы, обусловленные спинами электронов, скомпенсированы. Зато у свободных радикалов налицо электрон неспа-ренный. Именно этот признак и выдает присутствие осколка молекулы. Препарат свободного радикала парамагнитен. Он втягивается магнитным полем ё отличие от целостных органических соединений. Те диамагниты: их поле выталкивает В опыте Гомберга радикалы трифенилметила легко обнаруживались по их канареечно-желтой окраске. А если они не отличимы по цвету от сопутствующих соединений? И если их так мало, что невозможно взвесить в магнитном поле? Как тогда изучать свободные радикалы? Между тем изучать их интересно и важно. Любое уравнение реакции отражает лишь старт и финиш процесса. А что было иа промежуточных этапах? Что за пружины двигают взаимодействием? Каковы промежуточные продукты? Есть ли у реакции побочные русла? С какой скоростью развивается процесс во времени? Как зависит его скорость от температур, давлений и прочих факторов? Короче, какова кинетика реакции? Не ответишь на эти вопросы — не разработаешь технологию производства ни удобрений, ни полимеров, ни лекарств. Извлекать информацию о самых тонких тонкостях химического процесса помогают свободные радикалы. С их помощью ученые как бы пробираются за кулисы уравнения реакции, чтобы разобраться в интимнейших механизмах химического превращения. В конце 1955 года состоялось знаменательное заседание ученого совета Института химической физики АН СССР. Доктор химических наук, ныне академик Владислав Владиславович Воеводский выступил с интересной идеей. Поставить на службу химии незадолго до того открытое явление электронного парамагнитного резонанса) Метод ЭПР был в те годы, мягко выражаясь, далек от совершенства. Понятно, почему предложение Воеводского было встречено научной общественностью с известной долей осторожности. А ныне метод ши- Развствленная цепная реакция вина, горный обвал. роко принят на вооружение исследовательскими лабораториями всего мира. Именно он позволяет изучать свойства и повадки эфемерных осколков молекулы. Новый способ использует особенности неспаренного электрона. В магнитном поле свободные радикалы поглощают электромагнитную энергию на радиочастотах. Возникают спектры ЭПР. Вид кривых зависит от строения свободного радикала. Но все они имеют резонансный всплеск, весьма характерный для каждого вещества. Именно метод ЭПР 20 t(6i Чем меньше роковая «затравка», тем с большим трудом прививается экспериментальная лейкемия и мышей. Прививание 10 тысяч и меньшего количества клеток болезни не вызывает. количественно подтвердил теорию, которая стала ответом на другую загадку, взволновавшую ученых в начале нашего века. СВОБОДНЫЕ ЗАКОВАНЫ В ЦЕПИ! В наше время, в «век атома», пожалуй, нет на Земле человека, который не слышал бы о цепных реакциях. Но мало кто знает, что они были открыты сначала в химии. Это произошло еще в 1913 году — на тридцать лет раньше, чем был запущен первый атомный котел. Ученые заинтересовались очень простой с виду реакцией: Н2 + С12 2НС1. Достаточно солнечному зайчику упасть на сосуд со смесью хлора и водорода, как произойдет взрыв. Даже один-един-ственный квант световой энергии способен сыграть роль запала. Это никак не вязалось с эйнштейновским законом фотохимической эквивалентности: каждый квант способен вызвать лишь один элементарный акт химического превращения. Неужели вывод Эйнштейна не верен? Верен. Поставьте на попа друг за другом костяшки домино. Толкните первую фишку. Толчок один, а падает вся очередь. Так и в смеси На с СЬ. Поглощение одного светового кванта действительно сопровождается одной элементарной реакцией: СЬ-Mtv =С1-+-С1 (точками обозначен возбужденный неспа-ренный электрон). Осколки молекулы хлора начинают стремительную вереницу химических превращений: С1+Н2=» = НС1+Н; Н+С12=НС1+С1; С1 + Н2~ «НС1+Н... И так далее. К финишу приходит огромное количество молекул хлористого водорода. Цепная реакция! Разве только нераз-ветвленная. Каждый одновалентный атом, погребенный в молекуле НС1, оставляет лишь одного активного продолжателя начатого дела. Число частиц в каждом колене не возрастает. Коэффициент размножения равен единице. Но так бывает не всегда. В разветвленных цепных реакциях один активный центр порождает лавину себе подобных. Коэффициент размноже- 6 |








