Юный техник 1973-06, страница 16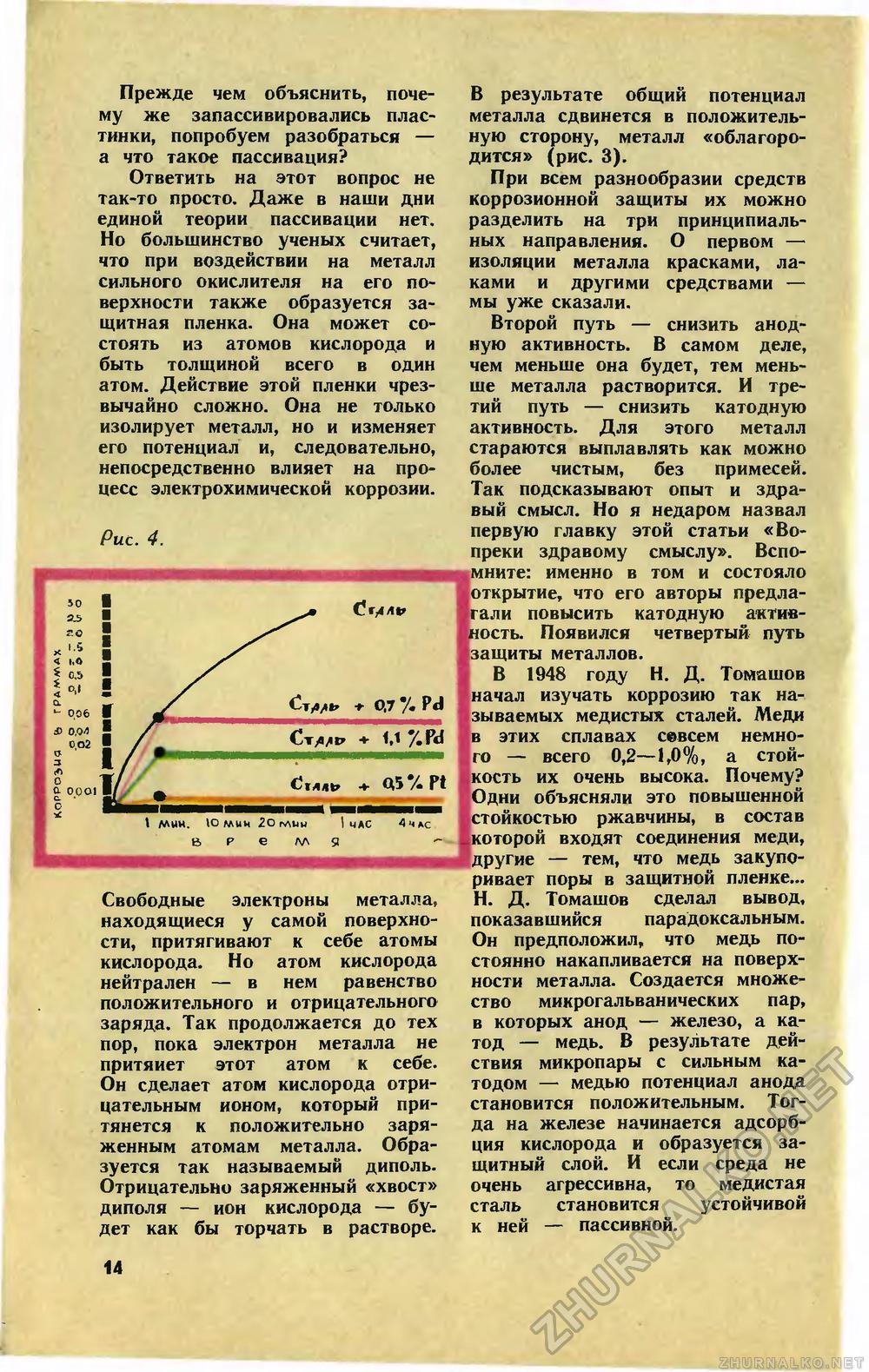
Прежде чем объяснить, почему же запассивировались пластинки, попробуем разобраться — а что такое пассивация? Ответить на этот вопрос не так-то просто. Даже в наши дни единой теории пассивации нет. Но большинство ученых считает, что при воздействии на металл сильного окислителя на его поверхности также образуется защитная пленка. Она может состоять из атомов кислорода и быть толщиной всего в один атом. Действие этой пленки чрезвычайно сложно. Она не только изолирует металл, но и изменяет его потенциал и, следовательно, непосредственно влияет на процесс электрохимической коррозии. Рис. 4. Свободные электроны металла, находящиеся у самой поверхности, притягивают к себе атомы кислорода. Но атом кислорода нейтрален — в нем равенство положительного и отрицательного заряда. Так продолжается до тех пор, пока электрон металла не притянет этот атом к себе. Он сделает атом кислорода отрицательным ионом, который притянется к положительно заряженным атомам металла. Образуется так называемый диполь. Отрицательно заряженный «хвост» диполя — ион кислорода — будет как бы торчать в растворе. В результате общий потенциал металла сдвинется в положительную сторону, металл «облагородится» (рис. 3). При всем разнообразии средств коррозионной защиты их можно разделить на три принципиальных направления. О первом — изоляции металла красками, лаками и другими средствами — мы уже сказали. Второй путь — снизить анодную активность. В самом деле, чем меньше она будет, тем меньше металла растворится. И третий путь — снизить катодную активность. Для этого металл стараются выплавлять как можно более чистым, без примесей. Так подсказывают опыт и здравый смысл. Но я недаром назвал первую главку этой статьи «Вопреки здравому смыслу». Вспомните: именно в том и состояло открытие, что его авторы предлагали повысить катодную активность. Появился четвертый путь защиты металлов. В 1948 году Н. Д. Томашов начал изучать коррозию так называемых медистых сталей. Меди в этих сплавах севсем немного — всего 0,2—1,0%, а стойкость их очень высока. Почему? Одни объясняли это повышенной стойкостью ржавчины, в состав которой входят соединения меди, другие — тем, что медь закупоривает поры в защитной пленке... Н. Д. Томашов сделал вывод, показавшийся парадоксальным. Он предположил, что медь постоянно накапливается на поверхности металла. Создается множество микрогальванических пар, в которых анод — железо, а катод — медь. В результате действия микропары с сильным катодом — медью потенциал анода становится положительным. Тогда на железе начинается адсорбция кислорода и образуется защитный слой. И если среда не очень агрессивна, то медистая сталь становится устойчивой к ней — пассивной. 14 |








