Техника - молодёжи 1947-09, страница 18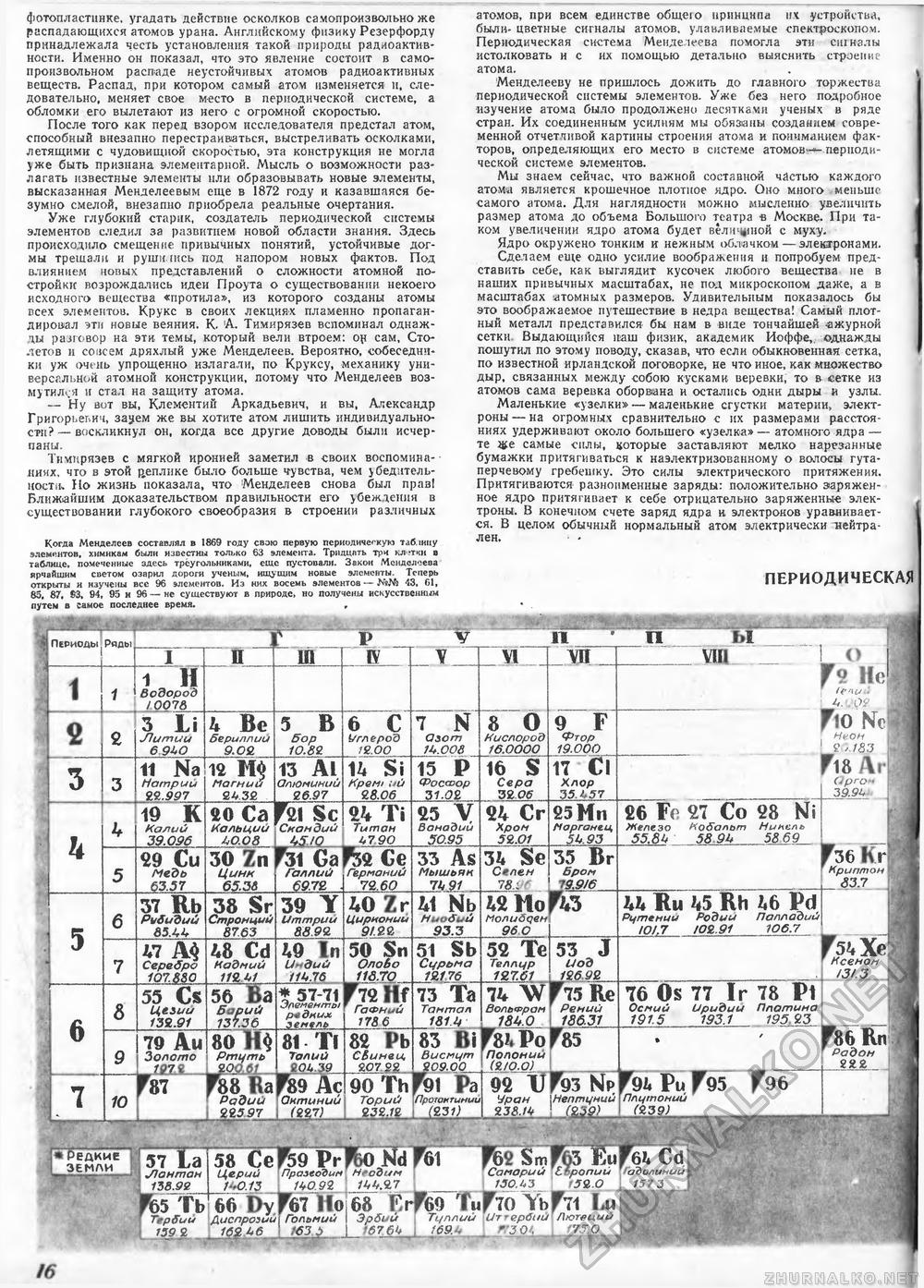
фотопластинке, угадать действие осколков самопроизвольно же распадающихся атомов урана. Английскому физику Резерфорду принадлежала честь установления такой природы радиоактив-ности. Именно он показал, что это явление состоит в самопроизвольном распаде неустойчивых атомов радиоактивных веществ. Распад, при котором самый атом изменяется н, следовательно, меняет свое место в периодической системе, а обломки его вылетают из него с огромной скоростью. После того как перед взором исследователя предстал атом, способный внезапно перестраишться, выстреливать осколками, летящими с чудовищной скоростью, эта конструкция не могла уже быть признана элементарной. Мысль о возможности разлагать известные элементы или образовывать новые элементы, высказанная Менделеевым еще в 1872 году и казавшаяся безумно смелой, внезапно приобрела реальные очертания. Уже глубокий старик, создатель периодической системы элементов следил за развитием новой области знания. чЗдесь происходило смещение привычных понятий, устойчивые догмы трешалм и рушились под напором новых фактов. Под влиянием новых представлений о сложности атомной постройки возрождались идеи Проута о существовании некоего исходного вещества «протила», из которого созданы атомы всех элементов. Крукс в своих лекциях пламенно пропагандировал эти новые веяния. К. 'А. Тимирязев вспоминал однажды разговор на эти темы, который вели втроем: ор сам, Столетов и совсем дряхлый уже Менделеев. Вероятно, собеседник ки уж очень упрощенно излагали, по Круксу, механику универсальной атомной конструкции, потому что Менделеев возмутился и стал на защиту атома. — 'Ну вот вы, Клементи и Аркадьевич, и вы, Александр Григорьевич, за^ем же вы хотите атом лишить индивидуальности? — воскликнул он, когда все другие доводы были исчерпаны. Тимирязев с мягкой иронией заметил в своих воспомияа- -днях, что в этой деплике было больше ч-увства, чем убедительности* Но жизнь показала, что Менделеев снова был прав! Ближайшим доказательством правильности его убеждения в существовании глубокого своеобразия в строении различных Когда Менделеев составлял в 1869 году сваю первую периодическую таблицу элементов, химикам были известны только 63 элемента. Тридцать три клетки в таблице, помеченные здесь треугольниками, еще пустовали. Закон Менделеева ярчайшим светом озарил дороги ученым» ищущим новые элементы. Теперь открыты и изучены все 96 элементов. Из них восемь элементов ~~ 43, 61, 83. 87, S3, 94, 95 и 96 — не существуют в природе, но получены искусственным путем в самое последнее время. , атомов, при всем единстве общего принципа их устройства, былй' цветные сигналы атомов, улавливаемые спектроскопом. Периодическая система Менделеева помогла эти сигналы истолковать и с их помощью детально выяснить строение атома, Менделееву не пришлось дожить до главного торжества периодической системы элементов. Уже без него подробное изучение атома было продолжено десятками ученых в ряде стран. Их соединенным усилиям мы обязаны созданием современной отчетливой картины строения атома и пониманием факторов, определяющих его место в системе атомов* периодической системе элементов. Мы знаем сейчас, что важной составной частью каждого атома является крошечное плотное ядро. Оно много меньше •самого атома. Для наглядности можно мысленно увеличить размер атома до объема Большого театра в Москве. При таком увеличении ядро атома будет величиной с муху. Ядро окружено тонким и нежным облачком — электронами. Сделаем еще одно усилие воображения и попробуем представить себе, как выглядит кусочек любого вещества не в наших привычных масштабах, не под микроскопом даже, а в масштабах «томных размеров. Удивительным показалось бы это воображаемое путешествие в недра вещества! Самый плотный металл представился бы нам в виде тончайшей ажурной сетки. Выдающийся наш физик, академик Иоффе,, однажды пошутил по этому поводу, сказав, что если обыкновенная сетка, по известной ирландской поговорке, не что иное, как множество дыр, связанных между собою кусками веревки, то в сетке из атомов сама веревка оборшна и остались одни дыры и узлы. Маленькие «узелки» — маленькие сгустки материи, электроны— на огромных сравнительно с их размерами расстояниях удерживают около большего «узелка» — атомного ядра — те же самые силы, которые заставляют мелко нарезанные бумажки притягиваться к наэлектризованному о волосы гута-перчевому гребешку. Это силы электрического притяжения. Притягиваются разноименные заряды: положительно заряженное ядро притягивает к себе отрицательно заряженные электроны. В конечном счете заряд ядра и электронов уравнивается. В целом обычный нормальный атом электрически "нейтрален. ■ * ПЕРИОДИЧЕСКАЯ и — шшшвтяшят и ш 1 II Водород /0078 6 3 Li Литии 6 9UO к Be бериллии 9.0£ 5 В бор 10.82 11 Na] Натрии гг.997 19 К Калий 39.096 49 Си Медь 63.57 37 Rb Рубидий 65Л4 т М Серебро 107. 880 55 CS Цезии 132.91 19 All Золото _4Й21_ 12 Магний «о Са Кальций ШОВ 13 At алюминий fSLX SC Снамдий мш 6 С Углерод 12.00 1 4 Si H'pQMt ий g 8.06 9U Ti Титан Ь7.90 30 Zn т Gar» Се Нчыи frtnmjt'j Пепм/JMiJU Цинн 38 Sr Стронций 87.63 48 Cd Кадмий 11% Ы 56 Ba Барий 137.36 т 8оПН§ Pfftl Ш Ra| Радий gg 597 Галлий 69.7В 39 Y Umrnpuu 88.99. U9 In индий ilhM * 57-71 Элемента/ роднил Германий 72.60 40 Zr Цирнонии 9/.Ж 50 Sti Олобо 116.70 81 Т! Талий g 0U.39 9 Ас Онтиний №7) Гп Hf ГаФНий 178 6 82 РЬ СЗимеи. &07Sg_ 1 N азот 1U.008 15 Р Фоссоор $1.02 £5 V Ванадии 50.95 зз As Мышь ян ъм hi Ыь Ниобий SX3 51 Sb Сурьма JJI1J6 73 Та Тантал 181М 8 О Кислород 16.0000 16 S Сера ЖОб 64 Сг Хром 52.01 83 Висмут 109.00 90 Th| Торий [ Я32М 1 Уран 238.1* Е Редкие ЭЕИЛИ 57 La 1 Лантан 138.99 35 Tb Тербий 159 2 58 Се Церий 1 J+0.13 _ ЩГРг | Пралесн 66 Dy , Диспрозии I Гольмий Празеодим Неодим 1Щ92 J±b&7 г67 Но 68 Ё т feSmi Самарий 130A3 \4*б Эрбий 'б? ел 34 Se Селен 78.96 W Но Молибден 96 О ' 52 Те Теллур 127.61 74 W Вольфрам 18^0 &Ро Полонии (9,10.0) п иГш ЫР /6 |








